- Які закони термодинаміки?
- Походження законів термодинаміки
- Перший закон термодинаміки
- Другий закон термодинаміки
- Третій закон термодинаміки
- Нульовий закон термодинаміки
Ми пояснюємо, що таке закони термодинаміки, яке походження цих принципів та основні характеристики кожного з них.

Які закони термодинаміки?
Закони термодинаміки (або принципи термодинаміки) описують поведінку трьох основних фізичних величин: температура, Енергія іентропія, які характеризують термодинамічні системи. Термін «термодинаміка» походить від грец термос, Що це означає "тепла», Ю динамо, Що це означає "сила”.
Математично ці принципи описуються а набір рівнянь, що пояснюють поведінку термодинамічних систем, визначених як будь-який об'єкт дослідження (з а молекула або a людина, доки атмосфера або окріп в каструлі).
Є чотири закони термодинаміки, і вони є вирішальними для розуміння фізичних законів всесвіту і неможливість певних явищ, як-от рух вічний.
Походження законів термодинаміки
Чотири принципи термодинаміка Вони мають різне походження, а деякі були сформульовані з попередніх. Фактично перша була встановлена друга, робота французького фізика та інженера Ніколаса Леонарда Саді Карно в 1824 році.
Однак у 1860 році цей принцип був знову сформульований Рудольфом Клаузіусом і Вільямом Томпсоном, а потім додавши те, що ми зараз називаємо Першим законом термодинаміки. Пізніше з’явився третій, також відомий як «постулат Нерста», оскільки він виник завдяки дослідженням Вальтера Нернста між 1906 і 1912 роками.
Нарешті, у 1930 році з’явився так званий «нульовий закон», запропонований Гуггенхаймом і Фаулером. Слід сказати, що не в усіх сферах це визнано справжнім законом.
Перший закон термодинаміки

Перший закон називається «Законом збереження енергії», оскільки він диктує, що в будь-якому системи ізольована від навколишнього середовища, загальна кількість енергії завжди буде однаковою, навіть якщо вона може бути перетворена з однієї форми енергії в різні. Або іншими словами: енергію неможливо створити чи знищити, а лише трансформувати.
Таким чином, віддаючи задану кількість теплоти (Q) фізичній системі, її загальну кількість енергії можна обчислити як відведене тепло мінусробота (W), що виконується системою на її оточенні. Виражається у формулі: ΔU = Q - W.
Як приклад цього закону уявімо двигун літака. Це термодинамічна система, яка складається з палива, яке хімічно реагує під час процесу горіння, виділяє тепло і виконує роботу (це змушує літак рухатися). Отже: якби ми могли виміряти кількість виконаної роботи та виділення тепла, ми могли б обчислити повну енергію системи і зробити висновок, що енергія в двигуні залишалася постійною під час польоту: енергія не створювалася і не руйнувалася, а змінювалася. з хімічна енергія до калорійна енергія ЮКінетична енергія (рух, тобто робота).
Другий закон термодинаміки
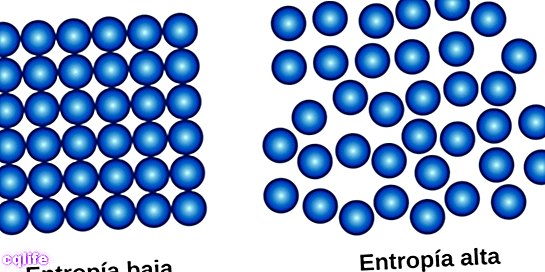
Другий закон, також званий «законом ентропії», можна підсумувати так, що кількість ентропія у Всесвіті має тенденцію до збільшення в погода. Це означає, що ступінь невпорядкованості систем зростає до досягнення точки рівноваги, яка є станом найбільшого невпорядкованості системи.
Цей закон вводить фундаментальне поняття у фізику: поняття ентропії (що позначається літерою S), яка у випадку фізичних систем представляє ступінь невпорядкованості. Виявляється, що в кожному фізичному процесі, в якому відбувається перетворення енергії, певна кількість енергії непридатна, тобто не може виконувати роботу. Якщо ви не можете виконувати роботу, то в більшості випадків це тепло. Те тепло, яке система виділяє, збільшує безладність системи, її ентропію. Ентропія - це міра невпорядкованості системи.
Формулювання цього закону встановлює, що зміна ентропії (dS) завжди буде рівною або більшою затеплопередача (dQ), поділена на температуру (T) системи. Тобто, що: dS ≥ dQ / T.
Щоб зрозуміти це на прикладі, достатньо спалити певну кількість матерія а потім зібрати отриману золу. Зваживши їх, ми переконаємося, що це менше матерії, ніж те, що було в початковому стані: частина речовини була перетворена в тепло у вигляді газів що вони не можуть працювати над системою і що вони сприяють її розладу.
Третій закон термодинаміки

Третій закон стверджує, що ентропія системи, яка доведена до абсолютного нуля, буде певною константою. Іншими словами:
- При досягненні абсолютного нуля (нуля в одиницях Кельвіна) процеси фізичних систем припиняються.
- При досягненні абсолютного нуля (нуля в одиницях Кельвіна) ентропія має постійне мінімальне значення.
Важко щодня досягти так званого абсолютного нуля (-273,15 °C), але ми можемо подумати про цей закон, аналізуючи те, що відбувається в морозильній камері: їжа що ми там депонуємо, охолоне настільки, що біохімічні процеси всередині нього сповільняться або навіть припиняться. Тому його розкладання затягується і його споживання набагато довше.
Нульовий закон термодинаміки
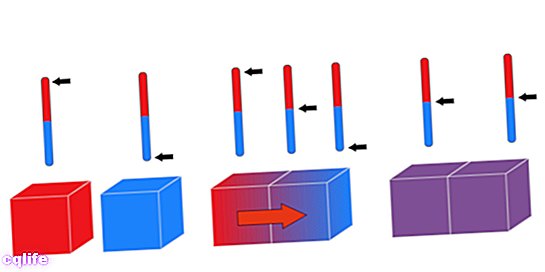
«Нульовий закон» відомий під такою назвою, хоча він був останнім. Також відомий як Закон теплової рівноваги, цей принцип диктує, що: «Якщо дві системи в теплова рівновага незалежно від третьої системи вони також повинні перебувати в тепловій рівновазі один з одним». Його можна логічно виразити так: якщо A = C і B = C, то A = B.
Цей закон дозволяє порівняти теплову енергію трьох різних тіл A, B і C. Якщо тіло A знаходиться в тепловій рівновазі з тілом C (вони мають однакову температуру), а B також має таку саму температуру, як і C, то A і B мають однакову температуру.
Інший спосіб сформулювати цей принцип — стверджувати, що коли два тіла з різними температурами стикаються, вони обмінюються теплотою, доки їх температури не вирівнюються.
Повсякденні приклади цього закону легко знайти. Коли ми потрапляємо в холодну або гарячу воду, ми помічаємо різницю в температурі лише протягом перших хвилин, оскільки потім наше тіло ввійде в теплову рівновагу зВода і ми більше не помічаємо різниці. Те саме відбувається, коли ми входимо в гаряче чи холодне приміщення: спочатку ми помічаємо температуру, але потім перестанемо сприймати різницю, тому що з нею увійдемо в теплову рівновагу.
