Аденозинмонофосфат являє собою нуклеотид, який може представляти частину носія енергії аденозинтрифосфату (АТФ). Як циклічний монофосфат аденозину, він також функціонує як другий месенджер. Він створюється, серед іншого, при руйнуванні АТФ, що звільняє енергію.
Що таке монофосфат аденозину?
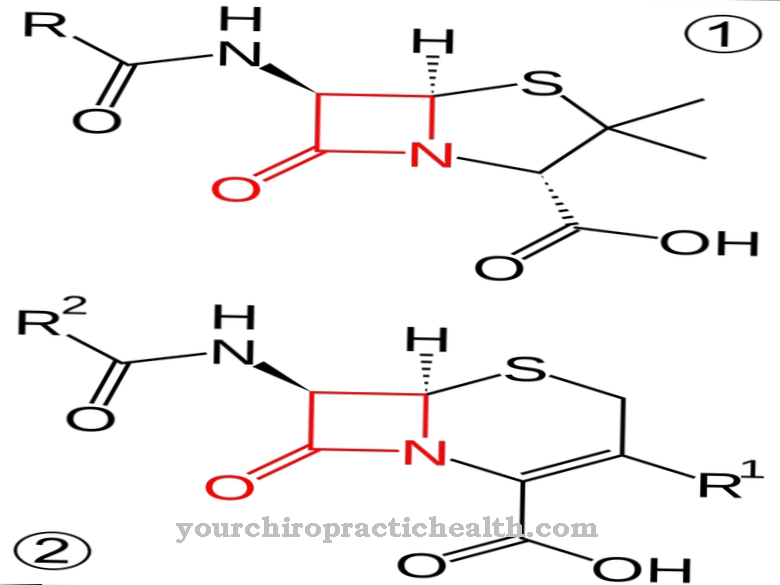
Монофосфат аденозину (C10H14N5O7P) є нуклеотидом і належить до пуринових риботидів. Пурин - це будівельний матеріал в організмі людини, який також міститься у всіх інших живих істотах. Молекула утворює подвійне кільце і ніколи не з’являється одна: Пурин завжди пов'язаний з іншими молекулами, щоб утворити більші одиниці.
Пурин - один із будівельних блоків аденіну. Ця основа також знаходиться в дезоксирибонуклеїновій кислоті (ДНК) і кодує генетично збережену інформацію. Крім аденіну, до пуринових основ належить також гуанін. Аденін в монофосфаті аденозину пов'язаний з двома іншими будівельними блоками: рибозою та фосфорною кислотою. Рибоза - це цукор з молекулярною формулою C5H10O5. Біологія також називає молекулу пентозою, оскільки вона складається з п'ятичленного кільця. У монофосфаті аденозину фосфорна кислота зв’язується з п'ятим атомом вуглецю рибози. Інші назви монофосфату аденозину - аденілат та аденілова кислота.
Функція, ефект та завдання
Циклічний аденозинофосфат (цАМФ) підтримує передачу гормональних сигналів. Наприклад, стероїдний гормон зв’язується з рецептором, який знаходиться на зовнішній стороні клітинної мембрани. У певному сенсі рецептор є першим реципієнтом клітини. Гормон і рецептор поєднуються разом, як ключ і замикаються, і, таким чином, викликають біохімічну реакцію в клітині.
У цьому випадку гормон є першим месенджером, який активує фермент аденілатциклазу. Цей біокаталізатор тепер розщеплює АТФ у клітині, створюючи цАМФ. Тоді цАМФ в свою чергу активує інший фермент, який, залежно від типу клітини, запускає реакцію клітин - наприклад, вироблення нового гормону. Монофосфат аденозину має функцію другого сигнального речовини або другого месенджера.
Однак кількість молекул не залишається однаковою від кроку до кроку: кількість молекул збільшується приблизно вдесятеро за крок реакції, що збільшує реакцію клітини. Це також причина, чому гормонів достатньо в дуже низьких концентраціях, щоб викликати сильну реакцію. В кінці реакції все, що залишається від цАМФ, - це аденозинмонофосфат, який інші ферменти можуть повернути в цикл.
Коли фермент розщеплює АМФ від аденозинтрифосфату (АТФ), утворюється енергія. Людський організм по-різному використовує цю енергію. АТФ є найважливішим носієм енергії в живих істотах і забезпечує, що біохімічні процеси можуть відбуватися на мікрорівні, а також рухи м’язів.
Монофосфат аденозину також є одним із будівельних блоків рибонуклеїнової кислоти (РНК). У ядрі клітин людини генетична інформація зберігається у вигляді ДНК. Щоб клітина могла працювати з нею, вона копіює ДНК і створює РНК. ДНК і РНК містять однакову інформацію в одному і тому ж розділі, але відрізняються за структурою їх молекул.
Освіта, виникнення, властивості та оптимальні значення
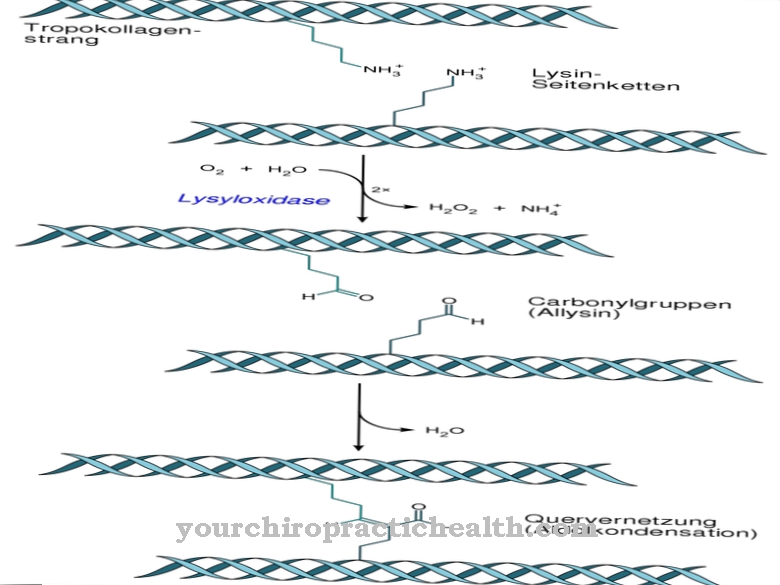
Монофосфат аденозину може виникати з аденозинтрифосфату (АТФ). Фермент аденилатциклаза розщеплює АТФ і вивільняє енергію в процесі. Особливо важливу роль відіграє фосфорна кислота речовин. Фосфоангідритні зв’язки з'єднують окремі молекули один з одним. Розщеплення може мати декілька можливих результатів: або ферменти розщеплюють АТФ на аденозиндифосфат (АДФ) і ортофосфат, або на АМФ і пірофосфат. Оскільки енергетичний обмін по суті нагадує цикл, ферменти також можуть поєднувати окремі будівельні блоки назад в АТФ.
Мітохондрії відповідають за синтез АТФ. Мітохондрії - це клітинні органели, які функціонують як електростанції клітин. Вони відокремлені від решти клітини власною мембраною. Мітохондрії успадковуються від матері (матері). Монофосфат аденозину є у всіх клітинах і тому його можна знайти скрізь у людському організмі.
Хвороби та розлади
Ряд проблем може виникнути з аденозинофосфатом. Наприклад, може порушуватися синтез АТФ в мітохондріях. Медицина також називає таку дисфункцію мітохондріальною хворобою. Він може мати різні причини, включаючи стрес, неправильне харчування, отруєння, пошкодження вільними радикалами, хронічні запалення, інфекції та кишкові захворювання.
Генетичні дефекти часто є причиною розвитку синдрому. Мутації змінюють генетичний код і призводять до різних порушень в енергетичному обміні або в структурі молекул. Ці мутації не обов'язково знаходяться в ДНК клітинного ядра; Мітохондрії мають свій генетичний склад, який існує незалежно від ДНК клітинного ядра.
При мітохондріопатії мітохондрії виробляють АТФ лише повільніше; Тому клітини мають менше енергії. Замість того, щоб будувати повний АТФ, мітохондрії синтезують більше АДФ, ніж нормально. Клітини також можуть використовувати АДФ для виробництва енергії, але АДФ виділяє менше енергії, ніж АТФ. При мітохондріальній хворобі організм може використовувати глюкозу як постачальник енергії; молочна кислота утворюється при їх руйнуванні. Мітохондріальна хвороба не є хворобою сама по собі, а є синдромом, який може бути частиною захворювання.
Медицина під назвою узагальнює різні прояви мітохондріальних розладів. Це може виникнути, наприклад, в умовах синдрому MELAS. Це неврологічне захворювання, яке характеризується судомами, ураженням мозку та підвищеним утворенням молочної кислоти. Крім того, мітохондріальна хвороба також пов’язана з різними формами деменції.
.jpg)


.jpg)



.jpg)
.jpg)